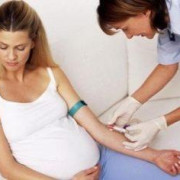
Подсадка эмбрионов при эко в деталях как происходит перенос
Содержание:
Смещение окна имплантации
В течение одного менструального цикла у женщины есть несколько дней, когда бластоциста способна прижиться в полости матки. Этот период называется окно имплантации. Поиск методик определения окна имплантации длится до сих пор. Распространение получил метод определения экспрессии более 200 генов в эндометрии. С помощью изучения этих генов ученые могут констатировать период, в течение которого эмбрион может прижиться в матке.
У женщин с повторными нерезультативными попытками экстракорпорального оплодотворения в 25% случаев было выявлено смещение окна имплантации (раньше или позже, чем ожидалось). Учитывая и используя на практике эту информацию, репродуктологи получают в 50% случаев факт наступления беременности у женщин с повторными нерезультативными циклами.
Полезная информация
Из каких этапов состоит культивирование эмбрионов?
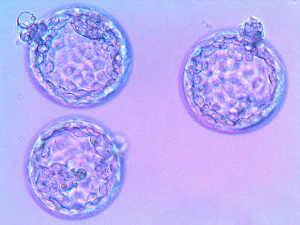
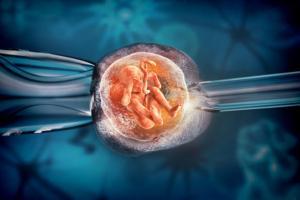
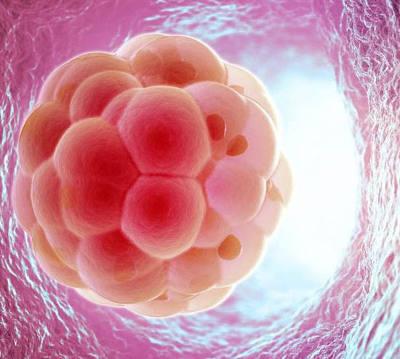
При успешном нормальном развитии после оплодотворения, в ходе доимплантационной жизни эмбрион должен пройти разные этапы развития. В норме на 2-е сутки эмбрион образует 4 клетки (бластомера), на 3 сутки — 8 клеток, затем происходит компактизация (слияние клеток), на 4 сутки образуется морула, которая затем на 5 сутки развивается в бластоцисты.
Эмбрион на стадии бластоцисты имеет сферическую форму и состоит из двух типов клеток — внутриклеточная масса и трофэктодерма. Трофэктодерма — наружный слой клеток, из которого впоследствии развивается плацента, а внутриклеточная масса — внутренний слой клеток, из которого затем развивается сам плод.
На каждом этапе доимплантационного развития эмбриона оценивается его качество, чтобы впоследствии выбрать на перенос наиболее перспективный для наступления беременности эмбрион. Качество эмбрионов в нашей лаборатории оценивается на 3 и 5–6 сутки развития. Эти дни наиболее информативны и оценка происходит по общепризнанным классификациям.
На 3 сутки оценивается количество образовавшихся бластомеров (клеток) эмбриона, их форма и размер, наличие или отсутствие фрагментации, степень фрагментации, наличие вакуолей и пр.

Фрагментация эмбриона — что это?
Фрагментация эмбриона — это отделение безъядерных (ануклеарных) фрагментов клеток эмбриона. При оценке качества эмбриона оценивается степень фрагментации выраженная в процентах.
Если фрагментация составляет более 35%, это может говорить о плохом качестве эмбриона, в дальнейшем приводящая к деградации эмбриона и остановке развития. Такой эмбрион не является перспективным для наступления беременности. При оценке качества эмбрионов, все показатели записываются в эмбриологический протокол для того, чтобы впоследствии выбрать наиболее перспективный эмбрион для переноса.
На 5 сутки при благополучном развитии эмбрион образует бластоцисту, состоящую из внутриклеточной массы и трофэктодермы. На данном этапе развития оценивается размер бластоцисты (степень экспансии), а также качество ВКМ и ТЭ, в соответствии с общепринятой классификацией.
Качество эмбрионов зависит от многих факторов. От качества исходно полученных клеток, от эмбриологического этапа, от генетических факторов, от возраста пациентов и особенностей анамнеза пациентов и пр. В случае получения плохих эмбрионов выбирается индивидуальная тактика. Эмбрион плохого качества имеет сниженные шансы на имплантацию и наступление беременности. Перенос такого эмбриона возможен, например, в случае отсутствия альтернативных вариантов.
Перенос эмбрионов осуществляется в свежем или крио цикле. Его можно проводить начиная со вторых суток развития, но оптимально — на 5 сутки, когда эмбрион сформировал бластоцисту. До этого момента есть возможность наблюдать динамику развития эмбрионов, чтобы впоследствии выбрать наиболее хорошо развивавшийся эмбрион и тем самым повысить шансы на беременность. В исключительных случаях перенос эмбриона осуществляется на 3 или 4 сутки.
| Название | Цена |
| Культивирование гамет и эмбрионов | 18500 руб. |
Указаны цены на самые востребованные услуги со скидкой 30%, которая действует при оплате наличными или банковской картой. Вы можете обслуживаться по полису ДМС, оплачивать отдельно каждый визит, заключить договор на программу ЭКО или внести депозит и получать услуги со скидкой. Услуги оказываются на основании заключенного договора.
Принимаются к оплате пластиковые карты MasterCard, VISA, Maestro, МИР. Также доступна бесконтактная оплата картами Apple Pay, Google Pay и Android Pay.

Что можно сделать, чтобы эмбрион прижился
Проводимое лечение (с целью повышения шансов прикрепления), выбирается с учетом морфологических изменений децидуальной ткани.

Для улучшения качества эндометрия при дефиците иммунной активности рекомендуют:
- локальное раздражение слизистой с помощью пайпель-биопсии (забор клеток эндометрия одноразовой трубочкой с боковым отверстием и поршнем внутри) или гистероскопии;
- умеренную овариальную стимуляцию;
- поддержку лютеиновой фазы низкими дозами препаратов хорионического гонадотропина;
- введение семенной жидкости после подсадки эмбрионов;
- внутриматочное введение периферических мононуклеаров, культивированных с хорионическим гонадотропином.
При повышенной иммунной активности возникает состояние, предшествующее воспалению, и эмбрионы не приживаются после переноса ЭКО.
Поэтому в этом случае рекомендуют:
- избегать локального раздражения слизистой матки;
- проводить стандартную овариальную стимуляцию;
- достаточную поддержку лютеиновой фазы;
- использовать кортикостероиды, интралипиды, внутривенное введение иммуноглобулинов;
- половой покой после переноса эмбриона;
- внутриматочное введение фолликулярной жидкости.
Почему не приживается эмбрион в матке с нарушенной децидуализацией
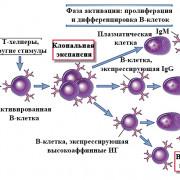
Эндометрий трансформируется в качественную децидуальную ткань во второй половине цикла при достаточном количестве прогестерона в плазме крови. Он пропорционально представлен иммунными клетками (NK-клетками и Тх).
Слизистая является разумным «детектором» качества эмбриона. Еще недавно считалось, что генетически «неправильный» зародыш не способен к длительному выживанию. На самом деле такой эмбрион способен продуцировать много биологически активных веществ. Он, таким образом, старается «понравиться» эндометрию.
Полноценный децидуализированный эндометрий – гормонально-зависимая ткань – «распознает» генетически измененный зародыш и перестает синтезировать для него целый ряд питательных веществ. Как результат – эмбрион останавливается в развитии. Природа спасает женщину от разочарований и прерывания беременности.
Существует два варианта нарушения децидуализации слизистой:
- сниженная локальная иммунная активность (недостаточное количество NK-клеток);
- повышенная локальная активность (отсутствует местная иммунорегуляция и чрезмерная мобилизация NK-клеток).
В результате нарушений эндометрий одинаково реагирует на полноценный и генетически измененный зародыш. Прикрепление неполноценного эмбриона в этом случае приводит к невынашиванию беременности. То есть, после ЭКО эмбрион не приживается, хотя и задерживается в матке на какое-то время.
Почему возникают мутации?
Мутации – не такое редкое явление, как многие считают. Около 70% эмбрионов не реализуются в беременность именно по причине генетических дефектов. Чаще всего после оплодотворения такая яйцеклетка погибает до имплантации. То есть, она не встраивается в стенку матки. Если же это происходит, велик риск самопроизвольного аборта. На определенном этапе плод перестает развиваться. Это обычно происходит в первом триместре, когда закладываются основные органы и ткани. Реже хромосомные мутации оказываются совместимыми с жизнью. Тогда у пары рождается больной ребенок.
Причины мутаций – это нарушение процесса дозревания яйцеклеток или сперматозоидов. В 85% случаев дефектные гены несут женские клетки, ещё в 15% – мужские. Причина заключается в том, что яйцеклетка – более сложная структура. Поэтому при её производства у организма больше шансов допустить ошибку.
Мутации могут быть спонтанными или наследуемыми. Хромосомные мутации обычно спонтанные. По наследству они передаются очень редко. А вот генные – наоборот, чаще наследуются. Таких заболеваний существует огромное количество. Проверить эмбрион на их все невозможно. Поэтому перед ПГД супружеская пара проходит генетическое консультирование, чтобы знать, какие именно болезни следует искать.
Когда риск генетических проблем у ребенка считается высоким?
Процедура ПГД не выполняется всем подряд. Её делают только тем, когда относят в группу. Таких групп две:
- родители, которые могут передать ребенку наследственную патологию;
- высокий риск образования анеуплоидных гамет при нормальном кариотипе.
ПГД при ЭКО всегда проводится носителям генных и хромосомных аномалий. Существует очень большая вероятность, что они будут переданы ребенку. Поэтому при проведении ПГД при ЭКО многие эмбрионы будут отбракованы. Их не станут переносить в матку. Соответственно, не родятся дети с генетическими или хромосомными мутациями, которые напрямую наследуются от родителей.
В число заболеваний, при которых делают ПГД эмбриона, входят:
- моногенные болезни: (аутосомно-рецессивные, аутосомно-доминантные, сцепленные Х‑ или Y половой хромосомой);
- структурные или числовые аберрации хромосом.
Пациенты с подозрением на мутации в хромосомах подлежат обследованию у генетика. Многие хромосомные патологии обнаруживаются в анализе крови, которые супруги могут сдать в случае повторяющихся неудачных ЭКО или привычных выкидышей. Однако иногда они в ходе генетической диагностики не выявляются. Бывают случаи механицизма – когда часть клеток у человека имеют хромосомные аберрации, а другие нормальные. В такой ситуации поможет консультация генетика, исследование материала абортусов или эмбрионов.
Вторая группа пациентов, нуждающихся в предимплантационной генетической диагностике, это люди с высоким риском по образованию анэуплоидных гамет. При этом у них может сохраняться нормальный соматический кариотип. То есть, набор хромосом в неполовых клетках соответствует норме.
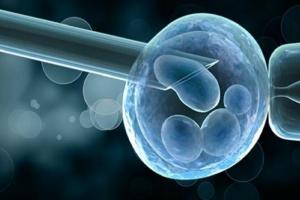
Такую генетическую диагностику называют предимплантационным скринингом. В ходе ПГД при ЭКО у всех эмбрионов считают количество хромосом, определяют их структуру. В разных клиниках используются разные диагностические подходы. Число хромосом, на которые проводят ПГД при ЭКО, может быть различным. Проверяют от 8 до 22 пары. При проведении генетической диагностики на меньшее количество хромосом проверяются те из них, в которых мутации бывают чаще всего. Если же используется максимальное исследование, оно может стоить дороже, но обнаруживает даже те аберрации, которые наблюдаются реже.
Установлено, что исследование всего 5 пар хромосом в ходе ПГД при ЭКО позволяет обнаружить 40% всех мутаций у эмбрионов, достигших стадии бластоцисты. Оценка состояния 12 хромосом обнаруживает 90% хромосомных перестроек.
В группу высокого риска по анэуплоидиям входят по возрасту, отягощенному анамнезу (неудачные ЭКО, выкидыши) или результатам спермограммы (тяжелые нарушения с выраженной олигоастенотератозооспермией с высокой вероятностью приведут к хромосомным аберрациям у плода). Поэтому такие пациенты нуждаются в генетической диагностике. Перед тем как направлять супругов на ПГД при ЭКО, стоит сделать анализ кариотипа.
На генетический скрининг приходится около 60% всех проводимых в мире ПГД при ЭКО. Эта процедура имеет высокую эффективность, так как многие неудачные попытки искусственного оплодотворения и минимум 50% всех выкидышей ранних сроков обусловлены именно хромосомными аберрациями эмбрионов.
День 2
Именно на второй день можно говорить о том, что из яйцеклетки и сперматозоида образовалась новая жизнь: произошло первое дробление зиготы, и будущий малыш — это две-четыре клетки-бластомера. Бластомеры, возникающие при первоначальном делении зиготы – не совсем обычные клетки: они обходятся без стадии клеточного роста, то есть эмбрион состоит из всё большего числа клеток, а вот его размер почти не увеличивается.
Специалисты различают четыре типа эмбрионов.
-
Тип А — эмбрион отличного качества без ануклеарных (безъядерных) фрагментов.
-
Тип В — эмбрион хорошего качества с содержанием ануклеарных фрагментов до 20%.
-
Тип С — эмбрион удовлетворительного качества с содержанием ануклеарных фрагментов от 21% до 50%.
-
Тип D — эмбрион неудовлетворительного качества с содержанием ануклеарных фрагментов более 50%.
Причины отсутствия или несостоятельности имплантации
Существует несколько причин, по которым имплантация эмбриона после переноса становится безуспешной:
- Эмбрион останавливается в развитии. Причина – некачественный геном, сформировавшийся при оплодотворении.
- Нарушена рецептивность эндометрия. Причины – эндометриоз, полипы, последствия инфекционных воспалительных процессов, нарушения гормональной регуляции.
- Эмбрион самостоятельно не может избавиться от утолщенной белковой оболочки. Это часто происходит у возрастных пациенток и связано со старением яйцеклеток. Другие причины – подсадка эмбрионов после криоконсервации, длительная гормональная индукция овуляции, нарушение работы эндокринных органов, курение, культивация эмбриона в искусственной среде.
Когда лучше подсаживать эмбрион?
Подсадка возможна в любой день, с первого по шестой, и каждого выбора есть свои плюсы и минусы. Если поместить эмбрион в матку рано, на первый или второй день, то возможное негативное влияние искусственной среды будет минимизировано, но ведь и полость матки на таком сроке для будущего малыша не «дом родной», он должен был бы еще находиться в маточной трубе! К тому же на таком сроке еще невозможно оценить ни качество эмбриона, ни его подверженность генетическим заболеваниям.
На третий день можно уже уверенно отсеять нежизнеспособные эмбрионы, однако, для генетического анализа по-прежнему еще очень рано.
На четвертый, а особенно на пятый день оценить можно все: и жизнеспособность эмбриона, и генетические заболевания, которые он унаследовал. Наконец, именно в этот момент естественно зачатый малыш, а вернее – бластоциста, из которой он вы итоге разовьется, оказывается в полости матки. Так что именно в этот момент подсадка эмбриона наиболее удобна и естественна.
Плохо то, что к этому моменту искусственно оплодотворенные яйцеклетки уже несколько дней борются за жизнь «в пробирке» и больше половины в ходе этого жестокого соревнования «сходят с дистанции». Среди неудачников не только жертвы генетических мутаций, но и вполне здоровые и качественные эмбрионы, которые по неизвестным причинам замирают и останавливаются в своем развитии. Так что к часу «Х» может попросту не дожить ни один эмбрион.
Именно поэтому, хотя идеальным днем для подсадки мог бы стать день №4, ее осуществляют только на следующий день, или даже через день.
Наконец, еще один фактор, который приходится учитывать, — психологическое состояние мамы. Чем дольше она ждет переноса эмбриона, тем больше нервничает, и тем меньше шансы на удачную берменность.
Дорогие будущие мамы! Не нервничайте! Мы верим — все у нас получится!
11.03.2018
Подготовила Анна Первушина
ЭКО, физиология
Заболевания, мешающие прижиться эмбрионам после ЭКО
Есть ряд патологий и состояний, которые могут помешать прикрепиться эмбриону в полости матки:
- Наследственные и приобретенные тромбофилии (повышается уровень антифосфолипидных антител);
- Ожирение. Излишний вес негативно сказывается на созревании яйцеклеток и на имплантации.
- Возраст. Длительно считалось, что возраст не лучшим образом влияет на качество ооцитов. Но, оказывается, что возраст может препятствовать имплантации эмбрионов, полученных из донорских яйцеклеток. Исследования показали – после 45 лет достоверно снижаются имплантационные свойства внутренней оболочки матки.
- Иммунологические нарушения.
Когда началось использование ПГД в медицине?
Использование ПГД стало возможным только после того, как была разработана полимеразная цепная реакция, позволяющая анализировать структуру ДНК. Кроме того, проведение этой дополнительной вспомогательной репродуктивной технологии невозможно без ЭКО.
Поэтому впервые ПГД была использована в 1989 году. Был проведен анализ бластомера (клетки) эмбриона, пребывающего на стадии дробления. Он состоял из 6-8 одинаковых клеток. Процедура была выполнена успешно. У супружеской пары, имевшей повышенный риск Х-сцепленного заболевания, в 1990 году родился здоровый ребенок.
В 1992 году впервые была проведена ПГД моногенного заболевания (муковисцидоз). Некачественный эмбрион был отбракован. Женщине перенесли эмбрион без генетических заболеваний и мутаций, и у неё родился здоровый ребенок.
В 2012 году для диагностики хромосомных аномалий начал широко применяться метод FISH. С этого момента метод сравнительной гибридизации стал вытесняться из медицинской практики.
Кому требуется ПГД?
Ежегодно в России тысячи детей рождаются после ЭКО. Но не всегда во время этой процедуры выполняется преимплантационная генетическая диагностика. ПГД проводится по показаниям. Основные из них:
- носительство хромосомной аберрации или генетического заболевания у одного или обоих будущих родителей;
- возраст женщины более 35 лет;
- возраст мужчины 40 и более лет;
- тяжелые нарушения сперматогенеза у мужчины;
- привычное невынашивание беременности (2 и более случая перинатальных потерь в анамнезе);
- 3 и более неудачных попыток ЭКО;
- необходимость предотвращения возможного резус-конфликта;
- отягощенный семейный анамнез (выкидыши, мертворождения, хромосомные мутации и т.д. среди ближайших родственников супругов).
Возраст женщины – один из весомых факторов риска генетических аномалий у ребенка. Поэтому даже при отсутствии в анамнезе перинатальных потерь и неудачных ЭКО, после 35 лет лучше провести ПГД.
По статистике, риск рождения ребенка с хромосомными аберрациями составляет для женщин разного возраста:
- в 30 лет – 0,26%;
- в 40 лет – 1,6%;
- в 45 лет – 5,26%.
Таким образом, в 45 лет одна из 19 беременностей заканчивается выкидышем или рождением больного ребенка по причине хромосомных перестроек. Эти последствия можно предотвратить с помощью ПГД.
Условия имплантации при ЭКО
Механизм имплантации эмбрионов после переноса (при ЭКО) – теоретически не имеет отличий. Процесс малоизученный даже в естественных циклах. Известно, что он может растянуться во времени и состоит из двух основных фаз: прилипания и адгезии (или проникновения).
Необходимые условия для успешного прикрепления оплодотворенной яйцеклетки после ЭКО:
Активное взаимодействие эмбриона и эндометрия. Обеспечивается при полноценности зародыша и подготовленности клеток слизистой матки.
Вовремя произведенный перенос.
У репродуктологов существует такое понятие, как имплантационное окно. Это период, в течение которого матка способна взаимодействовать с зародышем. Имплантационное окно ограничено во времени, поэтому результативность ЭКО во многом зависит от своевременности трансфера в матку.
Пик рецептивности – способности клеток эндометрия взаимодействовать с эмбрионом – приходится на 20–21 день цикла, но может сдвигаться в зависимости от используемых препаратов для стимуляции, чувствительности организма к ним и длительности менструального цикла. Чаще всего имплантационное окно открывается на 20–21 день в естественном цикле, при контролируемой стимуляции овуляции – на 19–20, при заместительной гормональной терапии – на 21–22 день.
Важно, чтобы эмбрион на стадии бластоцисты (5 день развития после оплодотворения) находился в матке с открытым имплантационным окном. Хетчинг или вспомогательный хэтчинг
Хетчинг или вспомогательный хэтчинг.
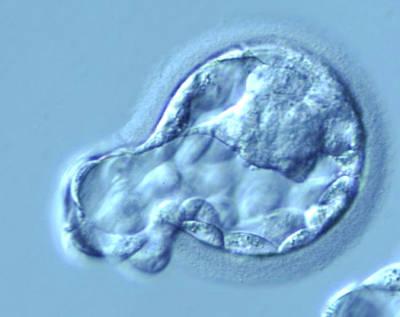
Блестящая (белковая) оболочка, окружающая эмбрион, мешает имплантации. Оказываясь в полости матки, зародыш больше не нуждается в ней. Бластоциста должна покинуть оболочку, иначе прикрепление на молекулярном уровне невозможно. Когда естественный процесс выхода из блестящей оболочки затруднен, в программах ЭКО прибегают к искусственному хетчингу.
Это интересно! Если отталкиваться от дня переноса пятидневного эмбриона, то имплантация при ЭКО происходит на 2-3 день. Это самый частый вариант, встречаемый в литературе. Но в протоколах возможно и более позднее прикрепление эмбриона – на 6-7 день, что называется поздней имплантацией.
Двойной перенос эмбрионов
Двойной перенос эмбрионов направлен на повышение шансов наступления беременности. Подсадка совершается двухмоментно:
- первый эпизод на 2–3 день культивации;
- второй – на 5–6.
За весь цикл может быть перенесено не больше 3-х зародышей.
Мнения об эффективности методики расходятся. С одной стороны, вероятность наступления беременности возрастает (более 50%), с другой – увеличивается угроза повреждения слизистой матки, уже подсаженных эмбрионов или смещение их в область маточных труб (на втором этапе ранее перенесенные и незакрепленные эмбрионы могут смываться раствором), с третьей – растут шансы многоплодия. Несмотря на это, во многих случаях, такой способ – альтернатива стандартной подсадки ЭКО.
Какие эмбрионы лучше приживаются: свежие или «крио»
Анализ свежих и «крио» циклов (перенос осуществляется в естественном цикле) показал закономерность, что частота беременностей в криопротоколах выше, чем в свежих протоколах. А частота выкидышей в свежих протоколах выше, чем в «криоциклах».

Крио эмбрионы лучше приживаются в матке. Кроме того, итальянские ученые подтвердили, что частота клинических и прогрессирующих беременностей в «крио» циклах выше, а частота выкидышей ниже.
Поэтому был сделан вывод, что замораживание эмбрионов и их перенос в естественном цикле (без стимуляции) является достаточно эффективной методикой и позволяет преодолеть неблагоприятные трансформации эндометрия, возникающие при стимуляции.
Влияние стимуляции на имплантацию
Весомой причиной того, почему эмбрионы не приживаются после ЭКО, является контролируемая овариальная стимуляция (КОС). Но необходимо сразу отметить, что точная причина и механизм изменений в матке, происходящий под влиянием КОС, мало изучен. Возможности гистологически исследовать эндометрий накануне переноса нет, так как при нарушении целостности слизистой эмбриотрансфер проводить нельзя (он будет неэффективным). То есть, получить материал для изучения вопроса – проблематично.
Исследования показывают, что в стимулированных циклах может наблюдаться преждевременный выброс прогестерона (еще до пункции фолликулов), который негативно сказывается на имплантационных свойствах эндометрия.
Уровень предимплантационных потерь после стимуляции овуляции, по сравнению с естественной беременностью, достоверно выше – это подтверждает неблагоприятное влияние КОС на имплантацию.
Сколько эмбрионов переносят при ЭКО
Однозначного ответа на этот вопрос нет. На то, сколько эмбрионов переносят при ЭКО, влияют: их качество, количество и возраст женщины. Согласно нормативным актам, пациенткам до 40 лет допускается перенос 3-х эмбрионов, после 40 – не более 4-х. Цель репродуктологов – максимально повысить шансы на имплантацию с последующим развитием беременности и одновременно избегать многоплодия. На практике чаще всего подсаживают 1–2 эмбриона.
В последнее время все чаще репродуктологи склоняются к тому, что нужно переносить 1 эмбрион, а не 2, ведь так заложено природой. Только в 1% случаев в естественных условиях развивается спонтанная двойня. Женский организм, его органы: сердце, почки, объем матки и таза «рассчитаны»на беременность одним эмбрионом, так зачем же идти против природы?
Гарантировано перенос 1 эмбриона осуществляется:
- при наличии рубца на матке от операции кесарево сечения;
- в программах суррогатного материнства (заказчики хотят «получить» здорового малыша, поэтому суррогатная мама должна вынашивать 1 ребенка);
- в донорских программах ЭКО.
https://youtube.com/watch?v=osxkhyRDSFc
Признаки имплантации эмбрионов после переноса и симптомы
Индивидуальные ощущения – головокружение, металлический привкус во рту, слабость, недомогание, повышение базальной и общей температуры тела, и другие сложно отнести к симптомам имплантации эмбриона после переноса. Они могут быть связаны с проводимой ранее индукцией овуляции, прогестероном, назначаемым для поддержки имплантации, или результатом «самокопания» – выискиванием признаков наступающей беременности.
Значимый признак имплантации эмбриона после переноса – имплантационное кровотечение, которое встречается редко. Его легко спутать с кровянистыми выделениями, происходящими из-за недостаточной поддержки лютеиновой фазы. Поэтому судить о природе их происхождения может лишь ваш доктор репродуктолог.
Как происходит оценка качества эмбрионов при ЭКО
Оценка качества эмбрионов при ЭКО происходит ежедневно. У ЭКО ИКСИ – есть преимущество – эмбриолог точно знает время оплодотворения в отличие от классического ЭКО, так как проводит процедуру самостоятельно. Это позволяет вести наблюдение за развитием с момента оплодотворения и оценивать эффективность развития более точно.

Сейчас существует оборудование, позволяющее вести запись дробления, которая используется для выбора самого качественного эмбриона. Характеристики, полученные при оценке, записываются в журнал, чтобы иметь возможность отслеживать динамику. Сразу после оплодотворения – слияния полярных телец яйцеклетка должна поделиться и образоваться два бластомера. Если этого не происходит или образуется больше клеток – эмбрион оценивается как некачественный.
Для определения хороший эмбрион или плохой существует много критериев:
- Внешний вид. Клетки должны быть правильной, равной и симметричной формы, внешняя оболочка – без утолщений.
- Соответствие дню развития по количеству клеток.
- Степень фрагментации – процентное соотношение безъядерных клеток (их еще называют кусочки цитоплазмы) к нормальным бластомерам (клеткам). Цитоплазматическая фрагментация бластомеров – это отсоединение от клетки фрагментов цитоплазмы, окруженной мембранной, но без ядерного содержимого. В норме каждый бластомер должен иметь ядро. Чем выше процент фрагментации, тем хуже прогноз для дальнейшего развития. Считается, что 25% фрагментации – вариант нормы. Часто мелкие фрагменты могут опять участвовать в дальнейшем построении других клеток. Фрагментация более 25% – признак снижения жизнеспособности. Тем не менее, фиксируются случаи, когда зародыши с высокой степенью фрагментации на 5 и 6 день становятся качественными или бластоцистами. Поэтому фрагментированные эмбрионы не отбраковываются а культивируются до 5–6 суток. У них есть шанс.
- Размеры. Клетки должны быть равными по объему и правильной формы.
- Наличие включений. Любые включения – неблагоприятный признак. Вакуоли – цитоплазматические включения, окруженные мембранной и содержащие жидкость, снижают частоту формирования хороших эмбрионов. Зиготы с выраженными вакуолями могут не вступать в дробление или происходит цитолизис – разрушение клеток.
- Равномерность деления, чем короче промежуток времени эмбрион имеет непарное количество бластомеров, тем лучше. Например, короткий промежуток между тремя и четырьмя клетками говорит о том, что два бластомера на двухклеточной стадии поделились равномерно. Кроме этого, деление должно происходить в определенное время.